¿QUE SON LAS SERIES HOMOLOGAS?
Serie Homóloga:
Una serie homóloga es una familia de compuestos orgánicos que contienen un particular
grupo de características y que muestran propiedades similares.
Por ejemplo , los compuestos que figuran a continuación pertenecen a la familia del los
alcoholes:
Alcohol metílico CH3OH ( metanol )
Alcohol propílico CH3CH2CH2OH ( 1 - propanol )
Alcohol butílico CH3CH2.CH2.CH2OH ( 1 - butanol )
Características de una serie homóloga
Todos los miembros de una serie homóloga presentan algunas características comunes.
Ellos son:
Todos los miembros de una serie homóloga pueden ser representados por
una fórmula general común , ya que tienen el mismo grupo funcional .
Por ejemplo , Los alcanos pueden ser representados por la fórmula CnH2n +2 .
Asi tenemos :
CH4 Metano
C2H5 Etano
C3H8 Propano
C4H10 Butano
Cada miembro de una serie homóloga tiene una diferencia común de -CH2
De los miembros del lado superior o inferior.
Existen métodos generales comunes de preparación para todos los miembros de la serie.
Todos los miembros tienen un comportamiento químico similar.
Un aumento de la masa molecular de los miembros dentro de una serie homóloga
muestra una graduación regular similar de las propiedades físicas , tales como ,
estado físico, puntos de fusión, ebullición , etc.
Puntos de ebullición y series homólogas
Conforme aumenta el número de átomos de carbono en una molécula en una serie homóloga, el punto de ebullición aumenta.
El punto de ebullición de alcanos de cadena lineal aumenta cuando se añade un grupo metileno (–CH2–) debido a que las fuerzas de van der Waals entre las moléculas aumenta al aumentar la masa molecular relativa del alcano.
Una tendencia similar se observa en los puntos de ebullición de otras series homólogas.
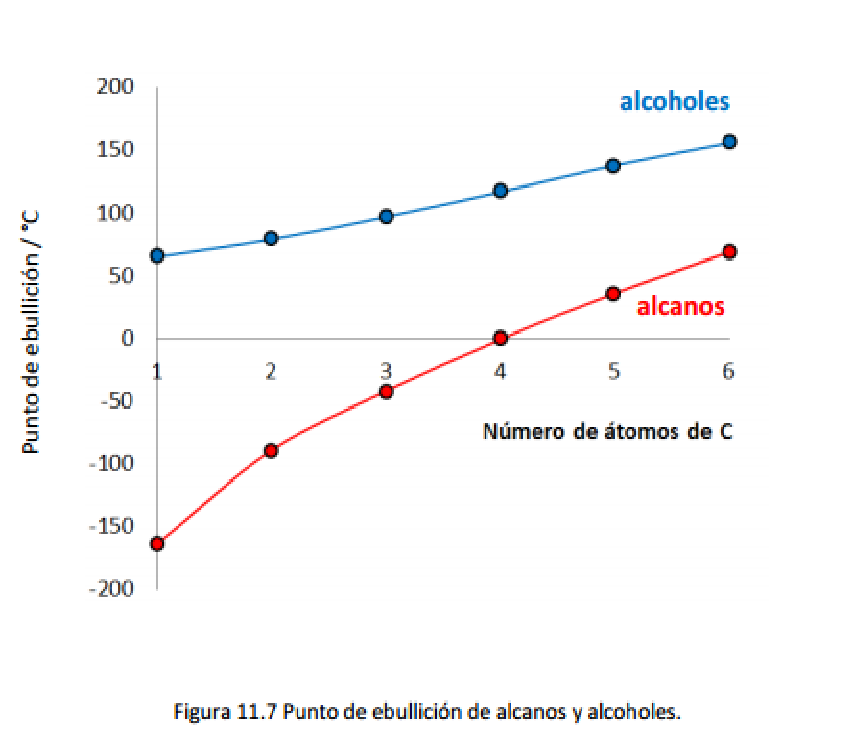
La Figura compara los puntos de ebullición de los alcoholes
(con el grupo funcional –OH en el primer átomo de carbono) con los puntos de ebullición de los alcanos.
Se puede ver que ambas series presentan la misma tendencia ya que el punto de ebullición aumenta conforme el número de átomos de carbono aumenta.
Es importante notar que las comparaciones basadas en la masa molecular relativa, y por ende en la intensidad de las fuerzas de van de Waals, se puede realizar dentro de una misma serie homóloga pero no entre series homólogas distintas.
Los puntos de ebullición de los alcoholes tienden a ser mayores debido a la presencia de enlace de hidrógeno entre moléculas de alcoholes.
Una serie homóloga es una familia de compuestos orgánicos que contienen un particular
grupo de características y que muestran propiedades similares.
Por ejemplo , los compuestos que figuran a continuación pertenecen a la familia del los
alcoholes:
Alcohol metílico CH3OH ( metanol )
Alcohol propílico CH3CH2CH2OH ( 1 - propanol )
Alcohol butílico CH3CH2.CH2.CH2OH ( 1 - butanol )
Características de una serie homóloga
Todos los miembros de una serie homóloga presentan algunas características comunes.
Ellos son:
Todos los miembros de una serie homóloga pueden ser representados por
una fórmula general común , ya que tienen el mismo grupo funcional .
Por ejemplo , Los alcanos pueden ser representados por la fórmula CnH2n +2 .
Asi tenemos :
CH4 Metano
C2H5 Etano
C3H8 Propano
C4H10 Butano
Cada miembro de una serie homóloga tiene una diferencia común de -CH2
De los miembros del lado superior o inferior.
Existen métodos generales comunes de preparación para todos los miembros de la serie.
Todos los miembros tienen un comportamiento químico similar.
Un aumento de la masa molecular de los miembros dentro de una serie homóloga
muestra una graduación regular similar de las propiedades físicas , tales como ,
estado físico, puntos de fusión, ebullición , etc.
Puntos de ebullición y series homólogas
Conforme aumenta el número de átomos de carbono en una molécula en una serie homóloga, el punto de ebullición aumenta.
El punto de ebullición de alcanos de cadena lineal aumenta cuando se añade un grupo metileno (–CH2–) debido a que las fuerzas de van der Waals entre las moléculas aumenta al aumentar la masa molecular relativa del alcano.
Una tendencia similar se observa en los puntos de ebullición de otras series homólogas.
La Figura compara los puntos de ebullición de los alcoholes
(con el grupo funcional –OH en el primer átomo de carbono) con los puntos de ebullición de los alcanos.
Se puede ver que ambas series presentan la misma tendencia ya que el punto de ebullición aumenta conforme el número de átomos de carbono aumenta.
Es importante notar que las comparaciones basadas en la masa molecular relativa, y por ende en la intensidad de las fuerzas de van de Waals, se puede realizar dentro de una misma serie homóloga pero no entre series homólogas distintas.
Los puntos de ebullición de los alcoholes tienden a ser mayores debido a la presencia de enlace de hidrógeno entre moléculas de alcoholes.
Series homólogas Y Grupos Funcionales
La tabla muestra varios grupos funcionales y la serie homologa respectiva.
Se puede utilizar ‘R’ para representar un grupo alquilo. Así, un ácido carboxílico en general se puede representar como ‘RCOOH’ y un aldehído como ‘RCHO’.



Comentarios